Quand vous remplissez une ordonnance pour un médicament générique, vous vous attendez à ce qu’il fonctionne aussi bien que la version de marque. Et pour cause : la FDA exige que les génériques soient rigoureusement équivalents. Ce n’est pas une question de prix ou de compromis. C’est une question de science, de contrôle et de transparence.
Qu’est-ce qu’un médicament générique vraiment équivalent ?
Un médicament générique n’est pas une copie approximative. Il doit être identique à la version de marque en trois points fondamentaux : la même substance active, la même dose, et la même forme de présentation - comprimé, capsule, solution injectable, etc. La FDA appelle cela l’équivalence pharmaceutique. Cela signifie que si vous prenez 10 mg de lisinopril dans un générique ou dans un Zestril, vous recevez exactement la même molécule, dans la même quantité, avec le même mode d’administration.
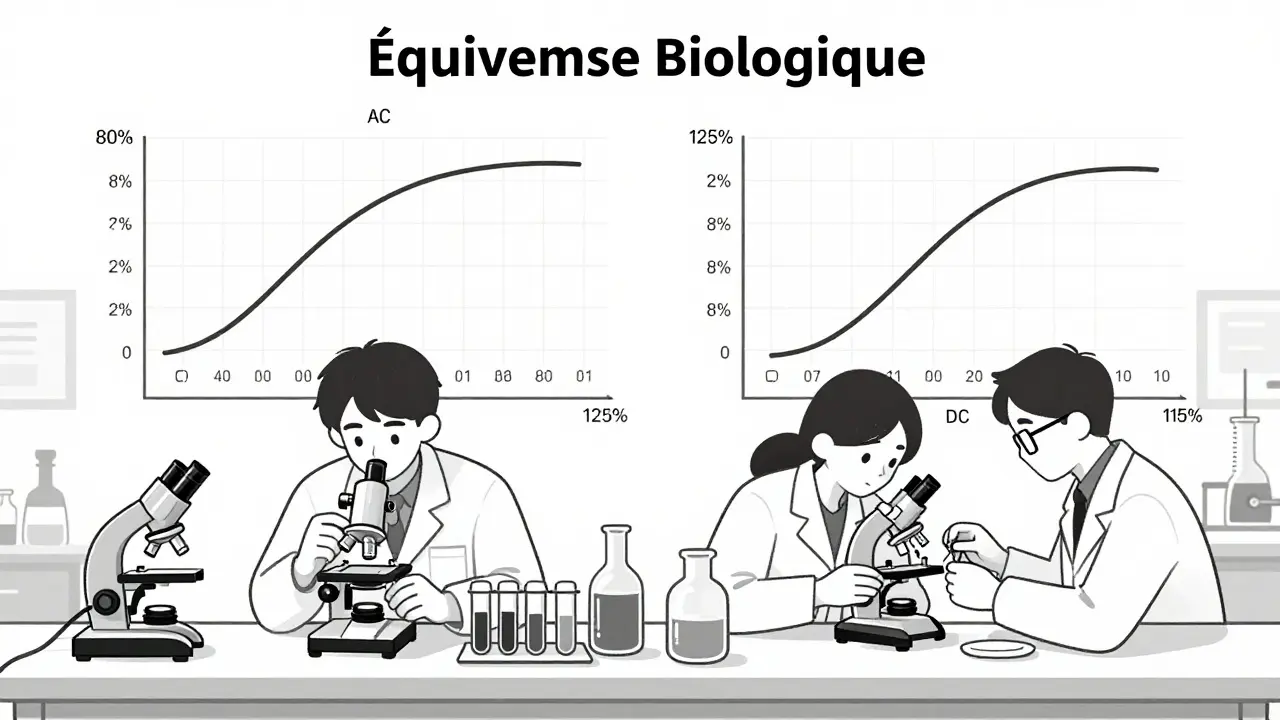
Mais ce n’est pas tout. Il faut aussi que le corps absorbe cette substance de la même manière. C’est là que vient l’équivalence biologique. La FDA exige que la vitesse et l’étendue d’absorption du générique soient dans une fourchette très précise par rapport au médicament de référence. Pour cela, les tests mesurent deux paramètres clés : la concentration maximale dans le sang (Cmax) et l’aire sous la courbe (AUC), qui représente la quantité totale absorbée. Les résultats doivent se situer entre 80 % et 125 % de la référence. Si un générique sort de cette zone, il n’est pas approuvé.
Comment la FDA vérifie tout ça ?
Le processus commence par une demande d’approbation appelée ANDA - Abbreviated New Drug Application. Contrairement aux médicaments de marque qui doivent passer par des essais cliniques complets, les génériques s’appuient sur les données existantes. Mais cela ne veut pas dire que c’est plus facile. Au contraire. L’ANDA doit inclure des preuves détaillées de la fabrication, de la pureté, de la stabilité et de la bioéquivalence.
Pour la bioéquivalence, la plupart des génériques sont testés sur 24 à 36 volontaires en bonne santé. On leur donne le générique et le médicament de marque, puis on mesure leur sang à intervalles réguliers pendant plusieurs heures. Les données sont analysées statistiquement pour s’assurer que les courbes d’absorption se chevauchent parfaitement dans la zone acceptée. Pour les produits complexes - comme les inhalateurs, les crèmes topicales ou les injections à action prolongée - les tests sont encore plus rigoureux. La FDA a publié plus de 2 100 directives spécifiques à chaque produit pour guider les fabricants dans ces cas particuliers.
Les normes de fabrication : pas de compromis
La qualité ne s’arrête pas à la composition. Elle commence à la matière première. La FDA impose les bonnes pratiques de fabrication (cGMP), qui s’appliquent à tous les fabricants, qu’ils produisent des médicaments de marque ou des génériques. Chaque lot doit être contrôlé pour vérifier :
- l’identité de la substance active
- la puissance exacte (est-ce bien 10 mg ?)
- la pureté (pas de contaminants, pas de résidus chimiques)
- la stabilité sur la durée de vie du produit
Les fabricants doivent faire des tests de stabilité accélérés : exposer les comprimés à 40°C et 75 % d’humidité pendant 6 mois pour simuler 2 à 3 ans de conservation. En parallèle, ils suivent les lots dans des conditions réelles pendant 12 à 24 mois. Si le médicament se dégrade trop vite, il est rejeté.
Et les installations ? La FDA inspecte environ 3 500 usines par an dans le monde entier. Ce n’est pas un contrôle ponctuel. C’est un suivi continu. Même les usines situées en Inde ou en Chine sont inspectées. Et sachez ceci : près de la moitié des génériques vendus aux États-Unis sont fabriqués par les mêmes entreprises qui produisent les médicaments de marque - dans les mêmes usines, avec les mêmes lignes de production.
Combien de génériques sont approuvés ?
En 2023, la FDA avait approuvé plus de 20 000 produits génériques, couvrant environ 14 800 médicaments de marque différents. Le système fonctionne. Plus de 90 % des ordonnances remplies aux États-Unis sont pour des génériques. Et pourtant, ils ne représentent que 23 % des dépenses totales en médicaments. C’est là que réside leur pouvoir : ils font baisser les coûts sans sacrifier la qualité.
En 2022, les génériques ont permis d’économiser 37 milliards de dollars au système de santé américain. Le marché américain des génériques, valorisé à 135,7 milliards de dollars en 2022, devrait atteindre 180,3 milliards d’ici 2027. Ce n’est pas une tendance. C’est une révolution silencieuse.
Et les problèmes ? Les exceptions réelles
La plupart des gens n’ont aucun problème avec les génériques. Un sondage de Consumer Reports en 2022 montre que 89 % des patients sont satisfaits. Mais il existe des cas spécifiques où la moindre variation peut avoir un impact.
Les médicaments à indice thérapeutique étroit - comme la lévothyroxine (pour la thyroïde), la warfarine (anticoagulant) ou certains anticonvulsivants - sont très sensibles. Une petite différence d’absorption peut entraîner des fluctuations de la concentration dans le sang. Une étude publiée dans JAMA en 2021 a montré que 12,3 % des patients ayant changé de générique de lévothyroxine ont dû ajuster leur dose à cause de changements dans leurs niveaux hormonaux.
Sur les forums de pharmaciens, comme Reddit, 17 % des réponses signalent des différences, principalement avec les médicaments pour l’épilepsie ou les troubles du rythme cardiaque. Ce n’est pas une preuve que les génériques sont mauvais. C’est une preuve que certains produits nécessitent une surveillance accrue. La FDA le sait. Elle a lancé des programmes spécifiques, comme le Pre-ANDA, pour aider les fabricants à mieux comprendre les exigences techniques avant de soumettre une demande. Depuis 2017, 18 ateliers publics ont réuni des centaines de scientifiques pour résoudre ces problèmes complexes.
Que dit la science ?
La FDA, l’American Medical Association, l’American Academy of Family Physicians - tous affirment la même chose : les génériques approuvés sont aussi sûrs et efficaces que les médicaments de marque. Dr. Janet Woodcock, ancienne directrice du Centre d’évaluation des médicaments, l’a dit clairement : « Les génériques approuvés par la FDA ont la même qualité, la même puissance, la même pureté et la même stabilité que les médicaments de marque. »
Et pourtant, le doute persiste. Pourquoi ? Parce que les gens confondent l’apparence avec la qualité. Un comprimé bleu au lieu d’un blanc, une forme ronde au lieu d’une ovale - cela ne change rien à la substance. Ce sont juste des différences dans les excipients (colorants, liants, etc.), qui n’ont aucun effet thérapeutique.
Le système a été conçu pour équilibrer deux objectifs : protéger les brevets des innovateurs, et permettre une concurrence juste pour rendre les médicaments abordables. Il fonctionne. Et il est soutenu par des données, pas par des opinions.
Que faire si vous avez un doute ?
Si vous avez déjà eu une réaction inattendue après un changement de générique, parlez-en à votre médecin ou à votre pharmacien. Ne changez pas de générique sans avis médical si vous prenez un médicament à indice thérapeutique étroit. Mais si vous n’avez pas de problème, continuez à les utiliser. Ils sont fiables, contrôlés, et économisent des milliards chaque année.
La prochaine fois que vous choisirez un générique, rappelez-vous : ce n’est pas une alternative. C’est la même chose. Juste moins cher. Et ça, c’est une bonne nouvelle pour tout le monde.
Les génériques sont-ils aussi efficaces que les médicaments de marque ?
Oui. La FDA exige que les génériques soient pharmaceutiquement et biologiquement équivalents aux médicaments de marque. Cela signifie qu’ils contiennent la même substance active, dans la même dose, et que le corps les absorbe de la même manière. Des études cliniques rigoureuses le confirment. Plus de 90 % des prescriptions aux États-Unis sont pour des génériques, et leur efficacité est prouvée depuis des décennies.
Pourquoi certains patients disent-ils qu’ils ressentent une différence ?
Dans la majorité des cas, ce sont des variations psychologiques ou des différences dans les excipients (couleur, forme, goût). Mais pour certains médicaments à indice thérapeutique étroit - comme la lévothyroxine, la warfarine ou certains anticonvulsivants - une petite variation d’absorption peut avoir un impact. C’est pourquoi la FDA exige des tests plus stricts pour ces produits. Si vous ressentez un changement, consultez votre médecin avant de changer de générique.
Les génériques sont-ils fabriqués dans les mêmes usines que les médicaments de marque ?
Oui, souvent. Environ 50 % des génériques aux États-Unis sont produits par les mêmes entreprises qui fabriquent les médicaments de marque, dans les mêmes installations, avec les mêmes équipements et les mêmes normes de contrôle. La FDA ne fait pas de distinction entre les deux. Ce qui compte, c’est la qualité du processus, pas le nom sur l’emballage.
Quelle est la durée de vie d’un générique ?
Les génériques doivent prouver leur stabilité sur toute leur durée de conservation, généralement de 2 à 3 ans. Les fabricants testent les lots sous des conditions extrêmes (chaleur, humidité) et en conditions réelles. Si le produit se dégrade, il est rejeté. La durée de péremption est la même que pour les médicaments de marque, et elle est strictement contrôlée par la FDA.
La FDA inspecte-t-elle les usines étrangères qui produisent des génériques ?
Oui. La FDA inspecte environ 3 500 usines chaque année, partout dans le monde - aux États-Unis, en Inde, en Chine, en Europe. Aucun médicament ne peut être importé aux États-Unis sans avoir passé ces inspections. Les usines qui ne respectent pas les normes sont mises sous surveillance, bloquées ou interdites. La qualité n’a pas de frontières.


10 commentaires
winnipeg whitegloves
Je trouve ça incroyablement rassurant de savoir que la FDA vérifie tout ça avec autant de rigueur. Les génériques, c’est pas une option économique, c’est une avancée scientifique. J’ai presque envie de faire un toast à chaque ordonnance remplie.
Caroline Bonner
Je suis vraiment impressionnée par la profondeur de cette explication - et franchement, je suis étonnée que tout le monde ne parle pas de ça en permanence ! Les tests de bioéquivalence, les 24 à 36 volontaires, les 2 100 directives spécifiques... C’est un système qui fonctionne comme une horloge suisse, et pourtant, les gens continuent de douter ! Il faut vraiment arrêter de confondre l’apparence avec la qualité - un comprimé bleu, ça ne change pas la molécule ! Et puis, les usines en Inde et en Chine ? Elles sont inspectées, vérifiées, surveillées - pas des ateliers de fortune !
Beau Mirsky
Oui, bien sûr... la FDA, c’est la bible. Mais qui vous dit que les données sont pas truquées ? Les labos ont des moyens... et les inspecteurs, ils sont payés par qui, déjà ?
Thibaut De Jaegher
En France, on a des génériques qui coûtent la moitié, et ça marche parfaitement. Pourquoi on se complique la vie avec des études américaines ? On a nos propres normes, et elles sont solides.
Louise jensen
Tout ça c’est du jargon pour faire peur aux gens. Bioéquivalence ? AUC ? Cmax ? Qui comprend vraiment ? Moi je prends mon générique, je vois pas de différence, et je m’en fiche. La science, c’est pour les gens qui aiment les tableaux Excel.
Valentin Duricu
90% des ordonnances ? Et alors ? Ça veut dire que 10% des gens ont eu un problème. Et ils sont silencieux.
Kim Girard
Ah oui, bien sûr, la FDA. Comme si les États-Unis étaient le temple de la santé mondiale. Et les essais sur 24 volontaires ? C’est un échantillon ridicule. On a des gens qui réagissent à des différences de 2% dans l’absorption. Et vous, vous croyez que ça se voit dans un graphique ?
Julie Ernacio
La vraie question, c’est pas si les génériques marchent. C’est pourquoi on nous pousse à les prendre. Qui gagne ? Les assureurs ? Les multinationales ? Le système ? Pas nous.
Nicole D
Même usine. Même ligne. Même contrôle. C’est tout.
Christophe MESIANO
Et si la FDA était corrompue ?